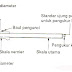
Elektrolit ( H2SO4 ).
Standard berat jenis ( specific gravity ) elektrolit battery pada temperature standard ( 200 Celsius ) adalah 1.280. Apabila temperature larutan elektrolit berubah, maka standard berat jenis dapat dicari dengan rumus:
Keterangan : S20 = Berat jenis pada temperatur 20 ° C
St = Berat jenis pada temperatur pengukuran
t = Temperatur electrolit pada saat pengukuran
Berat jenis akan turun pada saat battery dipakai ( discharge ). Pada kondisi standard ( 20 ° Celsius ), bila berat jenis elektrolit turun mencapai 1.20, maka battery harus diisi kembali ( charging ). Bila jumlah elektrolit di dalam battery berkurang, maka harus ditambah dengan air aki ( air suling ). Perubahan berat jenis elektrolit tergantung oleh :
- Discharge rate.
- Charge rate.
- Temperature.
- Jumlah asam sulfat yang terkandung dalam elektrolit.
Perubahan berat jenis ini dapat dilihat pada gambar - gambar berikut ini :
Larutan elektrolit dapat membeku pada temperatur tertentu. Oleh karena itu kalau menyimpan battery boleh ditempat sedingin mungkin asalkan tidak sampai .
Pembekuan
elektrolit pada berat jenis dengan
temperatur tertentu.
Jenis jenis Elektrolit :
• Asam Sulfat (H₂SO₄): Digunakan dalam baterai timbal-asam (lead-acid battery). Asam sulfat berfungsi sebagai elektrolit yang memfasilitasi reaksi kimia antara anoda (timbal, Pb) dan katoda (timbal dioksida, PbO₂).
• Kalium Hidroksida (KOH): Digunakan dalam baterai nikel-kadmium (NiCd) dan nikel-metal hidrida (NiMH). Kalium hidroksida berfungsi sebagai elektrolit dalam larutan basa.
• Larutan Garam Lithium: Digunakan dalam baterai lithium-ion (Li-ion). Elektrolit ini biasanya merupakan larutan garam lithium dalam pelarut organik seperti etilen karbonat atau dimetil karbonat.
Reaksi Kimia
Battery pada saat penggunaan maupun pengisian akan terjadi reaksi kimia berikut :
Yang dimaksud penggunan atau discharging dalam kapasitas battery.Reaksi kimia yang terjadi :
- Reaksi di elektroda negatif
Timbal bereaksi dengan ion hidrogen sulfat menghasilkan timbal sulfat, ion hidrogen, dan dua elektron.
- Reaksi di elektroda positif
Timbal dioksida bereaksi dengan ion hidrogen, ion sulfat, dan dua elektron menghasilkan timbal sulfat dan air.
- Reaksi keseluruhan saat proses penggunaan kapasitas battery adalah Timbal dan timbal dioksida bereaksi dengan asam sulfat menghasilkan timbal sulfat dan air.
b. Reaksi Kimia Pada Saat Pengisian.
Yang dimaksud proses pengisian atau recharging dalam kapasitas battery. Reaksi kimia yang terjadi ialah :
- Reaksi di elektroda negatif
Timbal sulfat menerima dua elektron dan berubah kembali menjadi timbal dan ion sulfat.
- Reaksi di elektroda positif
Timbal dioksida bereaksi dengan ion hidrogen, ion sulfat, dan dua elektron menghasilkan timbal sulfat dan air. Timbal sulfat dan air menghasilkan timbal dioksida, ion hidrogen, ion sulfat, dan dua elektron.
- Reaksi keseluruhan saat proses penggunaan kapasitas battery adalah Timbal dan timbal dioksida bereaksi dengan asam sulfat menghasilkan timbal sulfat dan air. Timbal sulfat dan air diubah kembali menjadi timbal, timbal dioksida, dan asam sulfat.
Larutan Elektrolit.
Baterai kendaraan mengandalkan elektrolit untuk mengalirkan listrik dan mendukung reaksi kimia yang menghasilkan energi. Asam sulfat, kalium hidroksida, dan larutan garam lithium adalah contoh elektrolit yang digunakan dalam berbagai jenis baterai kendaraan seperti berikut :
-
Asam Sulfat (H₂SO₄) pada baterai timbal-asam:
Menyediakan ion H⁺ dan HSO₄⁻ yang berpartisipasi dalam reaksi
kimia.
-
Kalium Hidroksida (KOH) pada baterai NiCd dan NiMH:
Mendukung reaksi redoks pada elektroda.
- Larutan Garam Lithium pada baterai Li-ion: Mengandung garam lithium seperti LiPF₆ yang dilarutkan dalam pelarut organik untuk memfasilitasi pergerakan ion lithium.
Setiap jenis baterai memiliki reaksi kimia spesifik yang memungkinkan penyimpanan dan pelepasan energi secara efektif.